皮肤真皮层内增生造成皮肤肿胀,继而变厚变硬,最终萎缩,还累及血管、肺、消化道、肾、心等器官造成内脏受损的表现。本病以皮肤受累范围为主要指标分为五型:弥漫性硬皮病、局限性硬皮病、无皮肤硬化的硬皮病、重叠综合征以及未分化结缔组织病。本病女性多见,发病率约为男性的4倍。
病因及病理
SSc的病因仍不清楚。通过复杂的遗传、环境、免疫、内皮细胞异常等因素的相互作用而导致疾病发生。SSc的特征性病理学表现为:众多血管床中小动脉和微动脉的增生性/闭塞性血管病。血管内层和中层肥厚与外层纤维化的同时存在导致管腔进行性变窄,加上内皮细胞的凋亡,最终导致闭塞性血管病变和血管稀少。
皮肤纤维化是SSc的标志,可伴随真皮层的显著增厚。随着疾病的进展,皮肤逐渐萎缩,表皮棘层变薄,钉脚消失。纤维化的真皮大部分无细胞成分,内含致密的透明胶原束、纤维蛋白和其他结构性基质蛋白的聚集物。汗腺和小汗腺腺体萎缩,腺体周围脂肪组织消失,导致皮下脂肪层消失。肺纤维化的特征是肺泡间质增厚,典型组织学表现为非特异性间质性肺炎。肺泡间隔进行性增厚,最终导致气道闭塞和蜂窝状改变,随后出现肺血管消失。肾以血管损害为主,以小叶间动脉和弓形肾动脉最明显,表现为弹力层增厚、内膜明显增生(葱皮样)和小动脉壁的纤维素样坏死,常伴微血管病性溶血。
临床表现
SSc常隐匿起病,发病年龄多在30~50岁。
雷诺现象
是SSc最多见的初期表现。临床特点为手指(足趾)端遇冷、情绪激动后出现麻木感和颜色顺序变化,首先是颜色变白,继以变紫,再变红。其原理在早期为局部小动脉痉挛,以后可因为血管内皮细胞肿胀导致组织缺血而出现指端溃疡及瘢痕,手(足)末节坏死或软组织及指骨因缺血而被吸收变短。
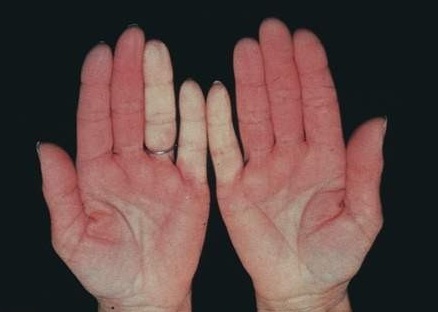
皮肤改变
是SSc标记性症状。皮损依次经历肿胀期、硬化期、萎缩期。早期肿胀期,手指呈腊肠样,手背非凹陷性肿胀。数周或数月后进入硬化期,皮肤呈蜡样光泽,厚而硬,紧贴于皮下,不易捏起。5~10年后进入萎缩期,浅表真皮变薄变脆,表皮松弛。皮下软组织钙化是SSc晚期并发症。手指端、肘、膝等易受外伤的部位是钙化好发之处。患者胸上部和肩部有紧绷感,颈前出现横向厚条纹,仰头时感颈部皮肤紧绷。面部皮肤受累典型表现为面具样面容。口周出现放射性沟纹,口唇变薄,鼻端变尖。面部、手臂和躯干可以出现皮肤色素脱失(白癜风样)和/或色素沉着(胡椒盐样外观)。即使未经日晒,也可出现皮肤晒黑的样子。手指的皮肤紧绷可逐渐导致指间关节和掌指关节完全伸展受限和屈曲畸形。毛细血管扩张表现为血管源性皮肤红色斑状损害,局部施压可以变白。它们主要累及手指、手、睑和黏膜,也可累及四肢和躯干。用毛细血管镜观察甲襞毛细血管异常,在硬皮病早期,可以看到扩张的毛细血管袢和微出血;在晚期阶段,甲襞毛细血管减少且排列混乱。
骨关节和肌肉
多关节痛和肌肉疼痛常为早期症状,也可出现关节炎。晚期由于腱鞘纤维化,受累关节活动时,可触到皮革样摩擦感。肌肉无力常见于严重皮肤病变者,多数因失用性萎缩造成。骨质吸收可见于末端指骨、肋骨、锁骨和下颌骨。
消化系统
消化系统受累是SSc的常见表现,任何部位均可累及,其中食管受累最常见,肛门、直肠次之,小肠和结肠较少。食管受累表现为上腹饱胀、胸骨后烧灼感,以及胃部反流。在平卧或弯腰时明显,是由于胃食管括约肌压力减低和远端食管扩张所致。1/3的SSc患者可有Barrett食管化生,这些患者发展为腺癌等并发症的危险性增高。胃部和肠道可出现毛细血管扩张,引起消化道出血。小肠蠕动减弱可导致肠胀气和腹痛,偶可出现假性肠梗阻。大肠受累导致慢性便秘,节段性肠道无力可导致肠套叠。肛门括约肌松弛可导致大便失禁,偶有肛门脱垂。
肺部
2/3以上的SSc患者有肺部受累,成为SSc最主要的致死原因。常见的症状是活动后气促,活动耐力减低,常伴干咳。肺间质纤维化和肺动脉血管病变常同时存在,但往往以一个病理过程占主导地位。肺间质纤维化常以嗜酸性肺泡炎为先导。在肺泡炎期,高分辨CT可显示肺部呈毛玻璃样改变,支气管肺泡灌洗液可发现细胞数增多,大多是肺泡巨噬细胞,可见到中性粒细胞或嗜酸性粒细胞。肺功能显示限制性通气障碍,肺活量降低,肺顺应性降低,气体弥散量减低。肺动脉高压是SSc的另一种严重肺部病变,是由于肺动脉和微动脉内膜纤维化和中膜肥厚导致狭窄和闭塞造成。肺动脉高压首先表现为劳力性呼吸困难,最终进展为右心功能衰竭。无创性超声心动检查可发现早期肺动脉高压。心导管检查发现33%的患者有肺动脉高压。
心脏
主要表现为心包炎,伴或不伴有心包积液、心力衰竭和不同程度的传导阻滞或心律失常。临床表现为气短、胸闷、心悸和水肿。超声心动图显示约半数患者有心包肥厚或积液。
肾
硬皮病肾病变以叶间动脉、弓形动脉及小动脉为著。临床表现不一,部分患者有多年皮肤及其他内脏受累而无肾损害的临床表现;有些在病程中出现肾危象,即突然发烧严重高血压、急性肾衰竭。如不及时处理,常于数周内死于心力衰竭和尿毒症。患者可出现乏力加重,气促、严重头痛、视力模糊、抽搐、神志不清等症状。实验室检查发现肌酐正常或增高、蛋白尿和/或镜下尿血,可有微血管溶血性贫血和血小板减少。少数患者可在没有高血压的情况下发生肾危象。
其他
SSc患者常伴眼干和/或口干症状。部分患者可出现甲状腺功能减低,可见甲状腺纤维化。偶见胆汁性肝硬化。
实验室和辅助检查
一般检查
血沉可正常或轻度增快。偶有贫血,可有轻度血清白蛋白降低,球蛋白升高。
免疫学检查
血清ANA阳性率达90%以上,核型为斑点型和核仁型。在CREST综合征患者中,约50%~90%抗着丝点抗体(ACA)阳性,在弥漫性硬皮病中仅10%阳性。ACA阳性患者常倾向于出现皮肤毛细血管扩张、皮下钙质沉积及肺动脉高压,较ACA阴性患者出现限制性肺部病变少。抗拓扑异构酶Ⅰ(Scl-70)抗体是SSc的特异性抗体,阳性率为15%~20%,该抗体阳性与弥漫性皮肤硬化,肺间质纤维化等相关。抗RNA聚合酶Ⅰ/Ⅲ抗体常与肾危象、心脏受累相关;抗PM-Scl抗体和抗Ku抗体见于局限性SSc重叠多发性肌炎的患者。抗SS-A和/或抗SS-B抗体存在于SSc与干燥综合征重叠的患者。
甲襞检查
甲襞电子毛细血管镜作为一种非创伤性的微血管检测方法已越来越广泛地应用于SSc患者的微血管病变评估、病情监测和疗效评估。早期表现为可见扩张/巨毛细血管,可见毛细血管出血,相对保留完好的毛细血管分布,以及没有毛细血管的缺失。活动期表现为巨毛细血管常见,毛细血管出血常见,毛细血管中度缺失,轻度毛细血管结构紊乱,没有或轻度分支毛细血管,存在水肿。晚期表现为不规则毛细血管扩张,少有或没有巨毛细血管和出血,严重的毛细血管缺失伴广泛地无血管区,正常毛细血管排列紊乱,以及分支或灌木丛样毛细血管的存在。
影像学检查及肺功能
胸片检查可有肺纹理增粗,严重时呈网状结节样改变,以肺底为著,或有小的囊状改变。高分辨CT和肺功能是检测和随访间质性肺病的主要手段。钡餐检查可显示食管、胃肠道蠕动减弱或消失,下端狭窄,近端增宽,小肠蠕动亦减少,近侧小肠扩张,结肠袋可呈球形改变。双手X线可见双手指端骨质吸收,软组织内有钙盐沉积。
超声心动图和右心漂浮导管检查
超声心动检查作为无创性的检查方法,是早期发现肺动脉高压的首选检查。但其敏感性和特异性较差。右心漂浮导管仍是诊断肺动脉高压的金标准。其可以测定肺血管阻力、心排出量,同时进行急性血管扩张试验和选择性肺动脉造影。
诊断
在2013年之前,使用最多的关于系统性硬化症的分类标准是由美国风湿病学会(ACR)于1980年制订的。该标准适用于长期的系统性硬化症患者,而早期的SSc以及局限性皮肤改变的患者被排除在外。自80年代以来,SSc相关的自身抗体和甲襞微血管异常变化逐渐被发现,而甲周微循环显微镜检查也逐渐成为一种为大众所接受的诊断工具。2013年11月ACR及欧洲抗风湿病联盟(EULAR)发表了SSc分类标准的最新修订版。该标准在1980年的基础上,增加了甲襞微循环异常和抗拓扑异构酶Ⅰ、抗RNA聚合酶Ⅲ抗体等内容,更有利于SSc的早期诊断。
1980年SSc分类标准,该标准包括以下条件。
主要条件。近端皮肤硬化:手指及掌指(跖趾)关节近端皮肤增厚、紧绷、肿胀。这种改变可累及整个肢体、面部、颈部和躯干(胸、腹部)。
次要条件:
①指硬化;
②指尖凹陷性瘢痕或指垫消失;
③双肺基底部纤维化。
判定:具备主要条件或2条以上次要条件者,可诊为SSc。雷诺现象、多发性关节炎或关节痛、食管蠕动异常、皮肤活检示胶原纤维肿胀和纤维化、血清有抗核抗体、抗Scl-70抗体和抗着丝点抗体阳性均有助于诊断。
| 主要标准 | 次要标准 | 权重/得分 |
| 双手手指延展至掌指关节的皮肤增厚(充分标准) | – | 9 |
| 手指肿胀 | 2 | |
| 手指皮肤增厚(只计最高分) | 指端硬化(掌指关节以远) | 4 |
| 指尖损害 | 指尖溃疡 | 2 |
| 指尖瘢痕小凹 | 3 | |
| 毛细血管扩张 | – | 2 |
| 甲襞微循环异常 | – | 2 |
| 肺动脉高压和/或间质性肺病 | 肺动脉高压 | 2 |
| (最高分不超过2分) | 间质性肺病 | 2 |
| 雷诺现象 | – | 3 |
| SSc相关自身抗体(最高分不超过3分) | 抗着丝点抗体 | |
| 抗拓扑异构酶Ⅰ | 3 | |
| 抗RNA聚合酶Ⅲ |
鉴别诊断
本病应与假性硬皮病,如硬肿病、硬化性黏液水肿、嗜酸性筋膜炎及肾源性系统性纤维化/肾源性纤维性皮病相鉴别。
治疗
虽然SSc的治疗有了较大进展,但有循证医学证据的研究仍然很少。皮肤受累范围及程度、内脏器官受累的情况决定其预后。早期治疗的目的在于阻止新的皮肤和脏器受累。而晚期的目的在于改善已有的症状。
一般治疗戒烟,加强营养,注意手足保暖和避免精神刺激。
对症治疗
SSc相关的指端血管病变(雷诺现象和指端溃疡)
二氢吡啶类钙离子挔抗剂,通常口服硝苯地平(10~20毫克/次,每日3次)可以用于SSc相关的雷诺现象的治疗。前列环素类似物可用于治疗SSc相关的严重的雷诺现象和局部缺血。口服波生坦也对治疗指端溃疡有效。
SSc相关的肺动脉高压
一般治疗:氧疗、利尿剂和强心剂以及抗凝治疗。
肺动脉血管扩张剂:临床上应用的血管扩张剂有钙离子拮抗剂(地尔硫卓),前列环素及其类似物(依前列醇、伊洛前列索、曲前列环素、贝前列环素),内皮素-1受体拮抗剂(波生坦、西他生坦、安立生坦)及5型磷酸二酯酶抑制剂(西地那非)等。
侵入性治疗:房间隔造口术,肺心联合移植和肺移植,肺血栓动脉内膜切除术。右心室辅助装置等。
SSc相关肾危象
肾危象可通过使用血管紧张素转换酶抑制剂(ACEI)来治疗。即使患者已经开始透析治疗,仍应继续使用ACEI。激素与SSc肾危象风险增加相关。使用激素的患者需要仔细的监测血压和肾功能。
其他脏器的治疗
长效质子泵抑制剂对胃食管反流性疾病、食管溃疡和食管狭窄有效。促动力药物如胃复安和多潘立酮可用于治疗SSc相关的功能性消化道动力失调如吞咽困难、胃食管反流性疾病、饱腹感等。
免疫抑制或抗纤维化治疗一些药物具有免疫抑制、抗纤维化作用或同时具有这两种作用,被用于治疗SSc。糖皮质激素可减轻皮肤病变水肿期的皮肤水肿和减轻关节和肌腱疼痛,但主张小剂量激素(10毫克/天或更小剂量)。大剂量激素使用(泼尼松>15毫克/天)与硬皮病肾危象显著相关。甲氨蝶呤可改善早期弥漫性SSc的皮肤硬化。其他药物如青霉胺、环孢素、他克莫司和静脉注射两种球蛋白对改善皮肤硬化可能有效。环磷酰胺被推荐用于治疗SSc的间质性肺病。霉酚酸酯对早期弥漫性病变有效。吡非尼酮可能成为新的抗纤维化治疗手段。
病程和预后
SSc的自然病程不一。在病情分化到特定亚型前,对早期病变的预后判断很困难。局限性硬皮病,尤其是抗着丝点抗体阳性者,预后良好,但是少数(<10%)患者在10~20年后并发肺动脉高压的例外。吸收不良综合征和原发性胆汁性肝硬化是部分局限性硬皮病患者的死亡原因。另一方面,弥漫性硬皮病患者的预后相对较差,尤其是晚年发病者。全身皮肤硬化快速进展者可能在病程早期就并发肾脏和其他脏器病变。肺、心脏和肾脏病变是常见死因。随着治疗肾危象有效药物的出现和肾衰竭透析治疗的发展,硬皮病肾危象的生存率明显提高。弥漫性硬皮病患者的5年生存率约70%,10年生存率约55%。局限性硬皮病的5年生存率约90%,10年生存率约75%。